
鹽酸
- 全國咨詢熱線:
- 15115761776
詳情介紹:
鹽酸是無色液體(工業(yè)用鹽酸會因有雜質(zhì)三價鐵鹽而略顯黃色),為氯化氫的水溶液,具有刺激性氣味,一般實驗室使用的鹽酸為0.1mol/L,pH=1。由于濃鹽酸具有揮發(fā)性,揮發(fā)出的氯化氫氣體與空氣中的水蒸氣作用形成鹽酸小液滴,所以會看到白霧。鹽酸與水、乙醇任意混溶,濃鹽酸稀釋有熱量放出,氯化氫能溶于苯。
20℃時不同濃度鹽酸的物理性質(zhì)數(shù)據(jù):
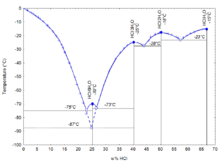
如下圖所示,鹽酸共有四個結(jié)晶的共熔點,分別對應(yīng)四種晶體:68%(HCl的質(zhì)量分數(shù),下同)時的HCl·H2O、51%時的HCl·2H2O、41%時的HCl·3H2O和25%時的HCl·6H2O。另外在24.8%時還有一種亞穩(wěn)的HCl·3H2O生成。
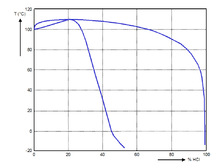
鹽酸在一定壓力下能形成共沸溶液。下圖為一個大氣壓下不同濃度鹽酸的沸點,其中下方的線與上方的線分別表示相應(yīng)溫度下,液體及與液體處于平衡狀態(tài)的蒸氣的組分。氯化氫的質(zhì)量分數(shù)20.24%對應(yīng)沸點108.6℃。
 化學性質(zhì)
化學性質(zhì)
酸性
鹽酸溶于堿液時與堿液發(fā)生中和反應(yīng)。
鹽酸是一種一元強酸,這意味著它只能電離出一個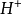
在水溶液中氯化氫分子完全電離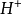
與一個水分子絡(luò)合,成為H3O+,使得水溶液顯酸性:

可以看出,電離后生成的陰離子是Cl-,所以鹽酸可以用于制備氯化物,例如氯化鈉。
鹽酸可以與氫氧化鈉酸堿中和,產(chǎn)生食鹽:

稀鹽酸能夠溶解許多金屬(金屬活動性排在氫之前的),生成金屬氯化物與氫氣:
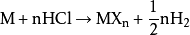
銅、銀、金等活動性在氫之后的金屬不能與稀鹽酸反應(yīng),但銅在有空氣存在時,可以緩慢溶解,例如:
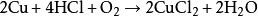
高中化學把鹽酸和硫酸、硝酸、氫溴酸、氫碘酸、高氯酸合稱為六大無機強酸。
一元酸只有一個酸離解常數(shù),符號為Ka。它能夠度量水溶液中酸的強度。于鹽酸等強酸而言,Ka很大,只能通過理論計算來求得。向鹽酸溶液中加入氯化物(比如NaCl)時pH基本不變,這是因為Cl-是鹽酸的共軛堿,強度極弱。所以在計算時,若不考慮極稀的溶液,可以假設(shè)氫離子的物質(zhì)的量濃度與原氯化氫濃度相同。如此做即使精確到四位有效數(shù)字都不會有誤差。
還原性
鹽酸具有還原性,可以和一些強氧化劑反應(yīng),放出氯氣:
二氧化錳:
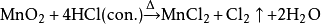
二氧化鉛:
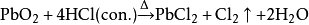
一些有氧化性的堿和鹽酸可以發(fā)生氧化還原反應(yīng),而不是簡單的中和反應(yīng):
配位性
部分金屬化合物溶于鹽酸后,金屬離子會與氯離子絡(luò)合。例如難溶于冷水的二氯化鉛可溶于鹽酸:
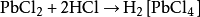
銅在無空氣時難溶于稀鹽酸,但其能溶于熱濃鹽酸中,放出氫氣:
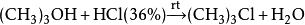
有機化學
酸性環(huán)境下可對醇類進行親核取代生成鹵代烴:
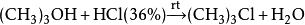
氯化氫也可以加成烯雙鍵得到氯代烴,例如:
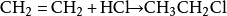
胺類化合物通常在水中溶解度不大。欲增大其溶解度,可以用稀鹽酸處理為銨鹽:
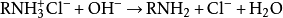
胺的鹽酸鹽屬于離子化合物,根據(jù)相似相溶原理,在水中的溶解度較大。銨鹽遇到強堿即可變回為胺:
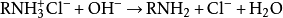
利用這樣的性質(zhì),可以將胺與其他有機化合物分離 。
此外,胺的鹽酸鹽的熔點或分解點可以用來測定胺的種類。
鋅粒與氯化汞在稀鹽酸中反應(yīng)可以制得鋅汞齊,后者與濃鹽酸、醛或酮一起回流可將醛酮的羰基還原為亞甲基,是為克萊門森還原反應(yīng):
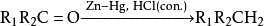
但應(yīng)注意,此法只適用于對酸穩(wěn)定的化合物,如果有α、β-碳碳雙鍵等也會被還原:
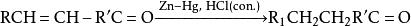
無水氯化鋅溶于高濃度鹽酸可以制得盧卡斯試劑,用來鑒別六碳及以下的醇是伯醇、仲醇還是叔醇。將盧卡斯試劑與叔醇立即渾濁,與仲醇2-5分鐘渾濁,伯醇加熱渾濁。
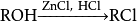
20℃時不同濃度鹽酸的物理性質(zhì)數(shù)據(jù):
| 質(zhì)量分數(shù) | 濃度 | 密度(Kg/L) | 物質(zhì)的量濃度 | 哈米特酸度函數(shù) | 粘性 | 比熱容 | 蒸汽壓 | 沸點 | 熔點 |
| (g/L) | (mol/L) | (m·Pa·s) | [KJ/(Kg·℃)] | (Pa) | (℃) | (℃) | |||
| 10% | 104.8 | 1.048 | 2.87 | -0.5 | 1.16 | 3.47 | 0.527 | 103 | -18 |
| 20% | 219.6 | 1.098 | 6.02 | -0.8 | 1.37 | 2.99 | 27.3 | 108 | -59 |
| 30% | 344.7 | 1.149 | 9.45 | -1 | 1.7 | 2.6 | 1410 | 90 | -52 |
| 32% | 370.88 | 1.159 | 10.17 | -1 | 1.8 | 2.55 | 3130 | 84 | -43 |
| 34% | 397.46 | 1.169 | 10.9 | -1 | 1.9 | 2.5 | 6733 | 71 | -36 |
| 36% | 424.44 | 1.179 | 11.64 | -1.1 | 1.99 | 2.46 | 14100 | 61 | -30 |
| 38% | 451.82 | 1.189 | 12.39 | -1.1 | 2.1 | 2.43 | 28000 | 48 | -26 |
如下圖所示,鹽酸共有四個結(jié)晶的共熔點,分別對應(yīng)四種晶體:68%(HCl的質(zhì)量分數(shù),下同)時的HCl·H2O、51%時的HCl·2H2O、41%時的HCl·3H2O和25%時的HCl·6H2O。另外在24.8%時還有一種亞穩(wěn)的HCl·3H2O生成。


酸性
鹽酸溶于堿液時與堿液發(fā)生中和反應(yīng)。
鹽酸是一種一元強酸,這意味著它只能電離出一個
在水溶液中氯化氫分子完全電離
與一個水分子絡(luò)合,成為H3O+,使得水溶液顯酸性:
鹽酸可以與氫氧化鈉酸堿中和,產(chǎn)生食鹽:
一元酸只有一個酸離解常數(shù),符號為Ka。它能夠度量水溶液中酸的強度。于鹽酸等強酸而言,Ka很大,只能通過理論計算來求得。向鹽酸溶液中加入氯化物(比如NaCl)時pH基本不變,這是因為Cl-是鹽酸的共軛堿,強度極弱。所以在計算時,若不考慮極稀的溶液,可以假設(shè)氫離子的物質(zhì)的量濃度與原氯化氫濃度相同。如此做即使精確到四位有效數(shù)字都不會有誤差。
還原性
鹽酸具有還原性,可以和一些強氧化劑反應(yīng),放出氯氣:
二氧化錳:
配位性
部分金屬化合物溶于鹽酸后,金屬離子會與氯離子絡(luò)合。例如難溶于冷水的二氯化鉛可溶于鹽酸:
酸性環(huán)境下可對醇類進行親核取代生成鹵代烴:
此外,胺的鹽酸鹽的熔點或分解點可以用來測定胺的種類。
鋅粒與氯化汞在稀鹽酸中反應(yīng)可以制得鋅汞齊,后者與濃鹽酸、醛或酮一起回流可將醛酮的羰基還原為亞甲基,是為克萊門森還原反應(yīng):







